稳定的亚胺前体-NOAc试剂应用于不对称Mannich反应
催化不对称Mannich反应作为有机合成中重要的C-C键构筑方式,广泛应用于合成化学中。其中,对于甲醛的不对称Mannich反应(也称为胺甲基化反应)以及乙醛酸酯的不对称Mannich反应是有效形成β-胺基羰基化合物以及α-氨基酸的手段,是当前最难的也是最迫切需要解决的问题。最近,中科院化学所分子识别与功能重点实验室罗三中课题组利用手性伯胺催化,结合合成的NOAcs试剂,成功实现了对于支链酮类化合物的不对称Mannich反应过程,以近乎光学纯的立体选择性高效地合成了一系列β-胺基羰基以及α-氨基酸酯类化合物(图1)。
|
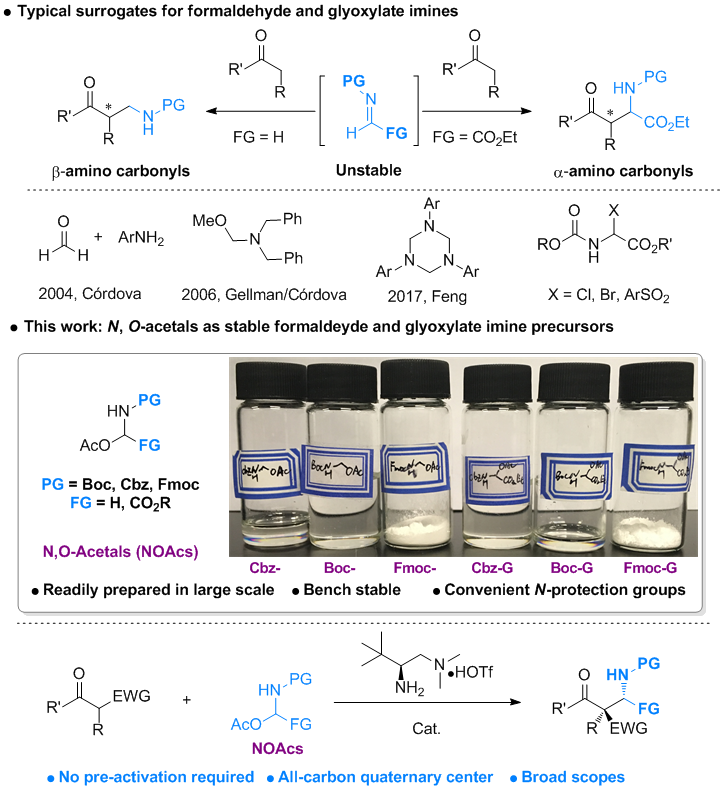
图1. NOAcs试剂作为亚胺前体 |
在最优反应条件下,作者首先对甲醛衍生的NOAcs试剂的反应底物范围进行了考察(图2)。各种β-酮羰基化合物均能很好的反应,并高立体选择性得到目标产物。
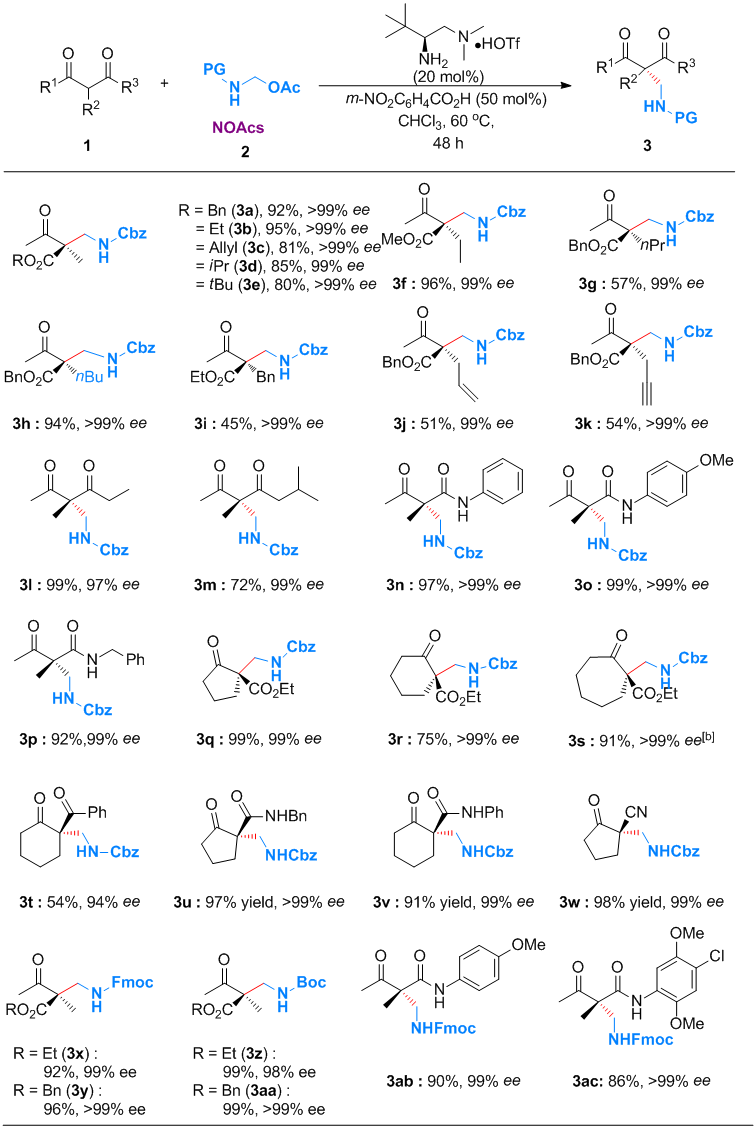
| 图2. 不对称胺甲基化反应底物范围 |
同时,作者也对乙醛酸酯衍生的NOAc-G试剂的反应进行了进一步探究(图3)。通过简单的优化,简单混合支链β-酮酸酯化合物与NOAc-G试剂在伯胺催化剂存在下就可以高选择性得到目标单一异构体。反应底物也可适用于α-氟代的酮酸酯以及α-未取代的酮羰基化合物,反应均得到很好的结果。值得注意的是,这样一个反应尤其适用于对称的二酮类底物,高选择性的得到目标产物。同时,反应也能很好的适用于简单的酮以及醛类底物,均表现出很高的选择性。
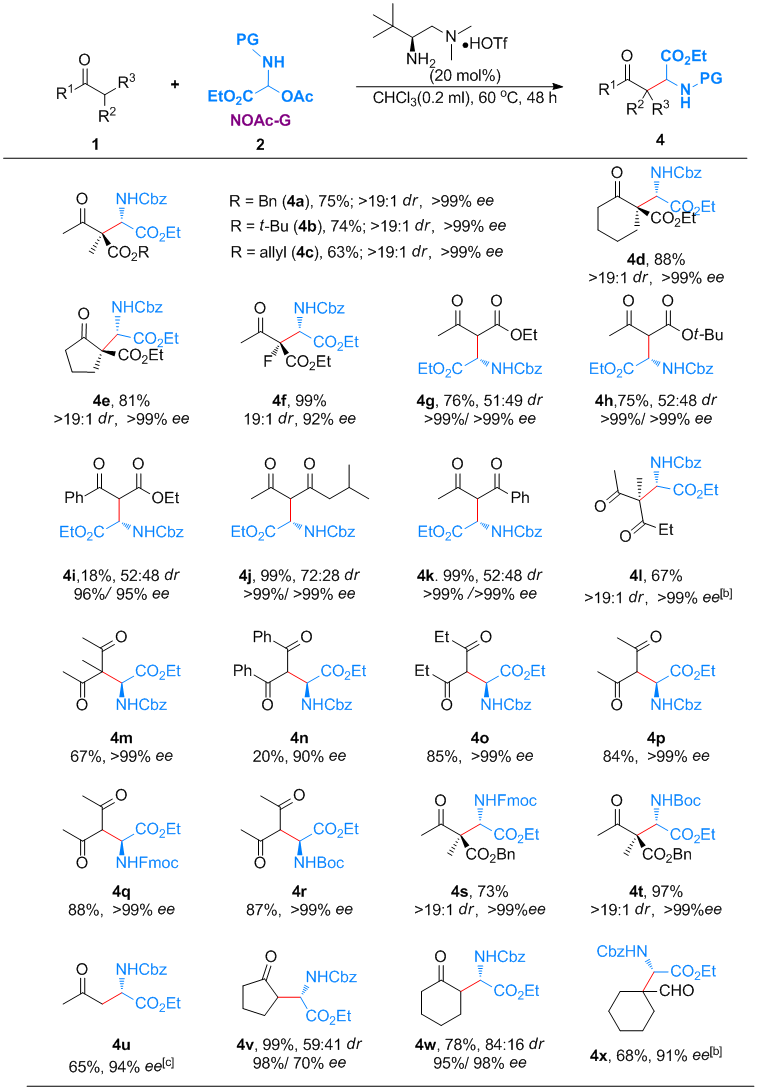
| 图3. NOAc-G试剂的不对称Mannich反应底物范围 |
基于实验的结果以及之前的研究(Angew. Chem. Int. Ed., 2014, 53, 4149-4153, Chem. Asian J., 2014, 9, 3565-3571.),作者提出了如下的反应过渡态(图4)。首先,NOAc试剂在伯胺催化剂的催化下原位产生亚胺中间体,烯胺从Re面与亚胺发生加成,质子化叔胺的N-H与亚胺之间的氢键决定了反应有很高的对应选择性以及非对应选择性。
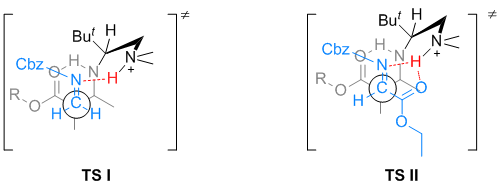
| 图4. 催化不对称Mannich反应的过渡态 |
在该工作中,罗三中研究员课题组设计合成了一系列由甲醛与乙醛酸酯衍生的稳定亚胺前体试剂,并将它们成功应用于对于醛酮α-位的不对称Mannich反应过程,高效立体专一地构建了手性的β-氨基酸与α-氨基酸类化合物。可以预见,这种通过N,O-缩醛替代亚胺作为稳定的亚胺前体的策略可以应用于更多官能化胺基手性中心的构建。
(该工作以“Catalytic Asymmetric Mannich Reaction with N-Carbamoyl Imine Surrogates of Formaldehyde and Glyoxylate”为题,发表在Angew. Chem. Int. Ed., 2017 , 56, 13814-13818.)

